Может ли терапия CytoSorb повлиять на концентрацию антибиотиков? Отчет о клиническом случае
Журнал "Антимикробная химиотерапия" (Journal of Antimicrobal Chemotherapy)
Цоллер М. (Zoller М)*1, Доббеллер Г. (Doebbeller G)1, Майер Б. (Maier B.)2, Фогесер М. (Vogeser M)2, Фрей Л. (Frey L)1, Зандер Й. (Zander J)2
1 Отделение анестезиологии, больница Университета Ludwig-‐Maximilians города Мюнхен, Мюнхен, Германия;
2 Институт лабораторной медицины, больница Университета Ludwig-‐Maximilians города Мюнхен, Мюнхен, Германия
Ключевые слова: мониторинг лекарственных средств, терапия антибиотиками, септический шок, бактериальные инфекции, меропенем, мониторинг терапевтических препаратов, отделения интенсивной терапии, in vivo, септицемия, линезолид
Адсорберы цитокинов, такие как CytoSorb® (производства Cytosorbents, Монмаут Джанкшн, штат Нью-Джерси, США), играют все более важную роль в терапии пациентов в критических состояниях, страдающих от воспалительного ответа. Адсорбция цитокинов позволяет сдерживать системное перепроизводство про- и противовоспалительных субстанций в условиях сепсиса.1 Недавно было показано, что BetaSorb® (производство компании CytoSorbents)элиминирует антибиотикив системе in vitro.2 Адсорбция жизненно важных антибиотиков системами, адсорбирующими цитокины in vivo, может привести к недостаточному или низкому уровню концентрации антибиотиков и неблагоприятному клиническому исходу, а также в конечном итоге может привести к формированию резистентности к антибиотикам. Однако, до настоящего времени данные in vivo по этому поводу недоступны. Здесь мы впервые, насколько нам известно, публикуем фармакокинетический мониторинг применения меропенема и линезолида in vivo во время терапии CytoSorb®.
Пациент с диагнозом септический шок и полиорганная недостаточность поступил в отделение интенсивной терапии (ОИТ) Университетской больницы Мюнхена. Состояние пациента характеризовалось широким воспалительным ответом: уровень лейкоцитов 1700/µл (диапазон нормальных значений 4000 – 11000/µл), 46 µг/л прокальцитонина (<0.1 µг/л) и 563 000 нг/л интерлейкина- 6 (<5.9 нг/л). Первая лапаротомия показала ишемию кишечника и перитонит. Пациенту безотлагательно был назначен меропенем (Meropenem) внутривенно (2 г), и проведена сегментарная резекция тощей кишки и кишечника с формированием илеотрансверзной колостомы. Результат анализа мазка показал наличие Enterobacteriaceae (меропенемчувствительной) и линезоид-чувствительного штамма Enterococcus faecalis. Через 5 часов после поступления пациента в ОИТ антимикробная терапия была дополнена препаратом линезолид (Linezolid). На этом этапе антибиотики вводились внутривенно с коротким периодом инфузии (15 – 60 минут).
Для остановки мощного цитокинового шторма было решено использовать дополнительную терапию с помощью системы CytoSorb®, содержащей горошины полимерного адсорбента. Терапия с помощью CytoSorb® проводилась 4 раза, общая ее продолжительность равнялась 96 часам. Первый сеанс терапии пришлось прервать, так как пациенту потребовалось еще одно оперативное вмешательство для достижения гемостаза. В течение последующих дней состояние пациента значительно улучшилось (было достигнуто улучшение функционирования почек и печени, а также кардиореспираторного статуса и др.). Однако, спустя 4 недели и 7 повторных процедур лапаротомии пациент скончался от полиорганной недостаточности.
Терапия
• 4 сессии терапии CytoSorb были проведено в течение в общей сложности 96 часов (1-ый день – 7 часов, 2-ой день – 10 часов, 3-ий день – 8 часов, 4-ый день – 5 часов).
Измерения
• Анализ концентраций антибиотиков в сыворотке (линезолид и меропенем) для определения потенциального вымывания их системой CytoSorb
• Удаление IL-6
В контексте обсервационного исследования (DRAK, ресурс Clinical Trials.gov, номер исследования: NCT01793012) для квантификации уровней линезолида были взяты образцы сыворотки. Образцы сыворотки брались из артериальной линии для определения концентрации антибиотиков во время рутинного забора крови до начала антимикробной терапии, во время и после ее проведения (в общей сложности было взято 25 образцов). Медицинский персонал записывал конкретное время взятия образцов. Образцы сразу же посылались в Институт Лабораторной Медицины, были центрифугированы и аликвотированы в полипропиленовые пробирки и помещены на хранение при температуре - 80 °С на 1 час. Концентрации линезолида в сыворотке определялись с использованием высокоточного метода LC-MS/MS (метод жидкостной хроматографии/тандемной масс-спектрометрии). Был принят следующий терапевтический диапазон для линезолида: от 2 мг/мл до 10 мг/л, 4, а для меропенема – 40% времени уровень в сыворотке выше 8 мг/л. 5
Рисунок 1 показывает значительное снижение уровня IL-6 за время четырех сессий терапии CytoSorb®: c 562 520 пг/мл в первые сутки до 19 394 пг/мл на четвертые сутки. Так как в результате критического состояния, постоперационного кровотечения и использования цитокинового фильтра была прописана высокая дозировка линезолида (4х600 мг в первые сутки) и меропенема (4 г на первые сутки), все измеренные концентрации антибиотиков значительно превышали нижний лимит терапевтического диапазона. Тем не менее, мы наблюдали у пациента высокую внутреннюю вариабельность уровней линезолида и меропенема (диапазон от низкого до высокого пика для линезолида составил 11.90 – 20.01 мг/л, а для меропенема= 38.4 – до 66.20 мг/л). Пиковые уровни линезолида были существенно более низкими (225 – 40%) во время сессии CytoSorb, по сравнению со смежными пиковыми уровнями. В конце концов, пиковый уровень меропенема во время второй сессии терапии CytoSorb был значительно ниже, чем пиковый уровень до использования.
Отмеченный значительно более низкий пик для препарата линезолид во время терапии CytoSorb® может быть результатом адсорбции цитокиновым фильтром. Действительно, сообщается о возможном поглощении цитокиновыми фильтрами различных эндогенных субстанций, помимо цитокинов.6 Адсорбция также объясняет более низкий пик меропенема во время второго применения CytoSorb®. Тем не менее, в этих исследованиях образцы крови для определения концентрации меропенема были взяты не в наилучшее для этого время, таким образом информация по поводу антибиотиков довольно ограничена. Нужно упомянуть, что высокая интраиндивидуальная вариабельность, зарегистрированная для обоих антибиотиков, может также являться результатом критического состояния. 4,7 Тем не менее, из-за возможной адсорбции антибиотиков цитокиновыми фильтрами терапевтический лекарственный мониторинг может быть особенно важен для пациентов, терапия которых дополняется подобными системами. На самом деле, первые директивы уже требуют наличия терапевтического лекарственного мониторинга для пациентов в критических состояниях.8,9 В случае если проведение терапевтического лекарственного мониторинга не представляется возможным, для достижения терапевтических концентраций рекомендуется использовать более высокие дозы или сокращать периоды между введением препарата. Полученный результат предполагает, что требуются дальнейшие исследования для понимания влияния цитокиновых фильтров на концентрации различных антимикробных препаратов.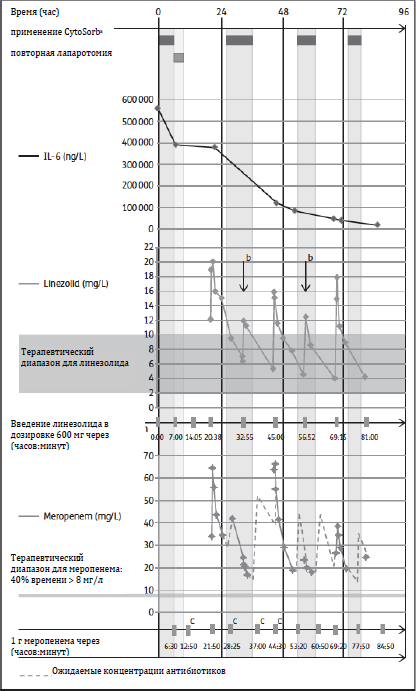
Рисунок 1. Влияние CytoSorb и антибиотиков на концентрации IL-6, линезолида и меропенема. Показаны первые 96 часов после начала терапии CytoSorb. a) Применение CytoSorb в соответствии с клиническими решениями. b) Более низкие пиковые уровни по сравнению со смежными пиковыми уровнями. c) Введение 2 г меропенема.
Выводы
• Впервые проведен фармакокинетический мониторинг линезолида и меропенема во время терапии CytoSorb
• Результаты показывают, что концентрации линезолида и меропенема в сыворотке могут снизиться при использовании CytoSorb, однако использование CytoSorb для этого пациента с тяжелым септическим шоком доказало свою эффективность (распад IL-6) и безопасность (уровни антибиотиков значительно выше нижней границы терапевтического диапазона)
Финансирование
Это исследование получило поддержку в виде гранта Мерье Ресерч (Merieux Research Grant) (Институт Мерье (Institut Merieux), Лион, Франция)
Ссылки
1 Белло Г. (Bello G), Ди Музио Ф. (Di Muzio F), Мавилья Р. (Maviglia R) et al. Новые мембраны для экстракорпоральной очистки крови при сепсисе Журнал Minerva Anestesiologica 2012; 78: 1265–81.
2 Райтер К. (Reiter K), Бордони В. (Bordoni V), Далл’олио Габриэль (Dall’Olio Gabriel) et al. Удаление терапевтических препаратов in-vitro новой адсорбирующей системой. Журнал «Очистка крови» (Blood Purification)2002; 20: 380–8.
3 Зандер Дж. (Zander J), Майер Б. (Maier B), Сухр А. (Suhr A) et al. Количественный анализ пиперациллина, тазобактама, сефепима, меропенема, ципрофлоксацина и линезолида в сыворотке с применением метода дилюции изотопов c помощью жидкостной хроматографии/тандемной массспектрометри (UHPLC-MS/MS) с полуавтоматической подготовкой образцов. Журнал «Клиническая химия и лабораторная медицина» (Clinical Chemistry and Laboratory Medicine) 2014; цифровой идентификатор объекта (doi):10.1515/cclm-2014-0746.
4 Золлер М. (Zoller M), Майер Б. (Maier B), Хорнусс Ц. (Hornuss C) et al. Вариабельность концентраций линезолида после стандартной дозировки у пациентов в критических состояниях: проспективное наблюдательное исследование. Журнал «Терапия критических состояний» (Critical Care) 2014; 18: R148.
5 Вонг Г. (Wong G), Бринкман А. (Brinkman A), Бенефилд РДж. (Benefield RJ) et al. Международный мультицентровый опрос по практике мониторинга терапевтического антибиотика b-лактам в отделениях интенсивной терапии. Журнал «Журнал Антимикробной терапии» (Journal of Antimicrobial Chemotherapy) 2014; 69: 1416–23.
6 Кунцевич В-И. (Kuntsevich VI), Файнфелд Д-А. (Feinfeld DA), Аудиа П-Ф. (Audia PF) et al. Клиренс миоглобина in-vitro с помощью новой сорбирующей системы. Журнал «Искусственные клетки, заменители крови и иммобилизационные технологии» (Artificial cells, blood substitutes, and immobilization biotechnology) 2009; 37: 45–7.
7 Робертс Дж.-А. (Roberts JA), Абдул-Азиз М-Х. (Abdul-Aziz MH), Липман Дж. (Lipman J) et al. Подбор индивидуальной дозировки препаратов для пациентов в критических состояниях: трудности и потенциальные решения. Журнал «Ланцет. Фактор влияния инфекционных заболеваний» (Lancet Infectious Diseases Impact Factor )2014; 14: 498–509.
8 Бодманн К-Ф. (Bodmann KF), Грабейн Б. (Grabein B). Рекомендации для расчетов парентеральной терапии инфекционных заболеваний для взрослых. Обновление 2010. Журнал «Химиотерапия» (Chemotherapy Journal) 2010; 19: 179–255.
9 Деллинер Р-П. (Dellinger RP), Леви М-М. (Levy MM), Родес А. (Rhodes A) et al. Выживание и борьба с сепсисом: международные принципы по управлению тяжелым сепсисом и септическим шоком: 2012 .Журнал «Медицина критических состояний» (Critical Care Medicine) 2013; 41: 580–637.

