Комбинированное применение CytoSorb и ЭКМО у пациентов с тяжелым пневмогенным сепсисом
Combined Use of CytoSorb and ECMO in Patients with Severe Pneumogenic Sepsis
Ali Akil1 Stephan Ziegeler2 Jan Reichelt1 Stephanie Rehers2 Omer Abdalla1 Michael Semik1 Stefan Fischer3
1 Department of Thoracic Surgery and Lung Support, Klinikum Ibbenbueren, Ibbenbueren, Germany
2 Department of Anesthesiology, Intensive Care Medicine and Pain Management, Klinikum Ibbenbueren, Ibbenbueren, NRW, Germany
3 Department of Thoracic Surgery and Lung Support, IbbenbuerenGeneral Hospital, Ibbenbueren, Germany
Опубликовано онлайн: 2020-04-06
Журнал Original Thoracic
Предпосылки В публикациях часто сообщается о высокой морбидности и летальности пациентов интенсивной терапии с тяжелым сепсисом и генерализованным воспалением. На фоне развития острого респираторного коллапса зачастую требуется применение экстракорпоральной мембранной оксигенации (ЭКМО). В настоящем исследовании пациентам с острым респираторным дистресс-синдромом (ОРДС) на фоне пневмогенного сепсиса в комбинации с ЭКМО применяли сорбцию цитокинов. Проводилась оценка эффективности этой терапии по сравнению с исторической когортой, где гемосорбцию не использовали.
Методы С января по май 2018 года пациентам (n13) с пневмогенным сепсисом и ОРДС проводили высокопоточную вено-венозную ЭКМО в комбинации с терапией CytoSorb (адсорбер включался в контур ЭКМО). Этих пациентов проспективно включали в исследование (группа CytoSorb). Группа контроля сформирована путем ретроспективного анализа пациентов (n7) с пневмогенным сепсисом, которым проводилась терапия ЭКМО.
Результаты В группе CytoSorb выжили все пациенты, в группе контроля 30-суточная летальность составила 57%. После проведения терапии CytoSorb мы наблюдали немедленное значительное снижение концентрации прокальцитонина (ПКТ) и С-реактивного белка (СРБ) по сравнению с контрольной группой. В группе CytoSorb, в отличие от группы контроля, в течение 48 часов назначение катехоламинов возможно было отменить.
Выводы Наши результаты указывают на то, что комбинация CytoSorb и ЭКМО является эффективной терапевтической методикой для предотвращения эскалации сепсиса и скорейшего окончания инфузии катехоламинов, наряду со стремительным снижением ПКТ и СРБ. Оптимальное время иммуномодулирующей терапии и ее влияние на ЭКМО-ассоциированное повреждение следует изучать далее.
Сепсис, развивающийся на фоне тяжелой инфекции, ассоциируется с высокой морбидностью и летальностью в отделениях интенсивной терапии.1,2 В случаях, когда происходит эскалация сепсиса или повторное его развитие, уровень летальности достигает 90-100%. При пневмогенном сепсисе развитие системного воспалительного ответа приводит к гемодинамической нестабильности и полиорганной недостаточности. Этот каскад ассоциируется c развитием острой дыхательной недостаточности с потребностью в ЭКМО.3 Однако, согласно представленным в литературе данным, процедура ЭКМО сама по себе способствует развитию синдрома системного воспалительного ответа (ССВО) с возникновением нарушений функционирования легких и сердечно-сосудистой системы. Терапия ЭКМО может выступать в качестве сверхстимулятора иммунной системы.4,5 Таким образом, необходим преимущественно оптимизированный подход для снижения интенсивности воспалительного ответа и деэскалации сепсиса.Дисрегуляция концентраций циркулирующих про- и противовоспалительных цитокинов играет ключевую роль в патогенезе сепсиса.2 Для предотвращения усугубления септических состояний и улучшения клинических исходов разработана адъювантная терапия - системы сорбции цитокинов. Целый ряд клинических и экспериментальных исследований продемонстрировал эффективность экстракорпоральной гемофильтрации для удаления цитокинов у описанной категории пациентов и оказание ей благоприятных воздействий на уровень выживаемости. 6-9 О положительном воздействии системы эстракорпоральной сорбции цитокинов CytoSorb (Cytosorbents Europe GmbH, Berlin, Germany) для контроля тяжелого сепсиса у реанимационных и кардиохирургических пациентов сообщалось в литературе. 7,8 Анализ международного реестра применений CytoSorb в различных клинических ситуациях, включающий [на момент написания этой статьи в 2019 г.] 20 исследовательских центров, дает основание предполагать, что терапию CytoSorb следует считать наилучшим адъювантным методом лечения сепсиса.9 Целью настоящего исследования являлось изучение эффектов, оказываемых сорбцией цитокинов на воспалительный ответ у пациентов с тяжелым пневмогенным сепсисом и дыхательной недостаточностью, требующей проведения ЭКМО, и сравнение этой группы с пациентами с тяжелым пневмогенным сепсисом, которым проводилась процедура ЭКМО без применения цитокиновой сорбции. Мы уже представляли данные о применении терапии CytoSorb у пациентов отделения интенсивной терапии во время 27-ой Европейской конференции по общей торакальной хирургии (27th European Conference on General Thorasic Surgery) в Дублине. Исследование проходило в период с января по май 2018 года.Все пациенты с септическим шоком и ССВО оценивались с точки зрения критериев включения и исключения настоящего исследования. Комбинация CytoSorb и ЭКМО применялась у пациентов с острой респираторной недостаточностью, развившейся на фоне пневмонии, и тяжелым пневмогенным сепсисом. Таких пациентов проспективно включали в исследование (в группу CytoSorb). Кроме того, мы регистрировали клинические параметры и собирали данные о клинических исходах исторической когорты пациентов нашего лечебного учреждения с острой дыхательной недостаточностью на фоне пневмогенного сепсиса, которым проводилась процедура ЭКМО и стандартная терапия в период до января 2018 года, когда система CytoSorb еще не была доступна в нашей клинике. Демография пациентов приведена в ►Таблице 1. Критерии включения и исключения приведены ниже.
Критерии включения
В исследование включали пациентов с пневмогенным септическим шоком и острой респираторной недостаточностью, потребностью в норэпинефрине 0.3мкг/кг/мин; подъемом концентрации лактата выше 2.0ммоль/л; ПКТ сыворотки выше 1 нг/мл гемодинамики. Соответствие критериям включения исследование оценивалась в течение 6 часов после поступления в отделение интенсивной терапии; при отсутствии улучшений при сохранении высокой потребности в норэпинефрине в первые 24 часа после развития септического шока
Таблица 1 Базовые характеристики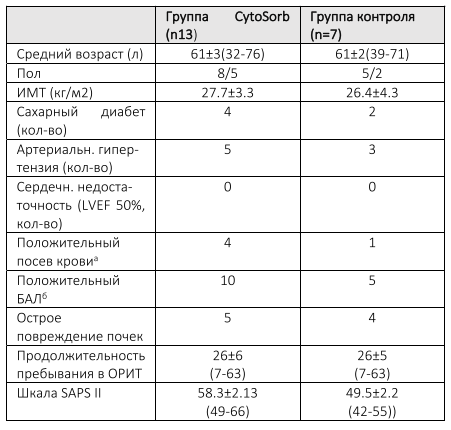 Сокращения: ИМТ – индекс массы тела; LVEF – left ventricular ejection fraction,
Сокращения: ИМТ – индекс массы тела; LVEF – left ventricular ejection fraction,
фракция изгнания левого желудочка; БАЛ – бронхоальвеолярный лаваж; ОРИТ
– отделение реанимации и интенсивной терапии; Шкала SAPS – Simplified Acute
Physiology Score.
a Культуральное исследование крови выявило рост Staphylococcus aureus (n 1),
Enterococcus faecium (n 1), Streptococcus pyogenes (n 1), Candida albicans (n 1) в
группе CytoSorb и Enterococcus faecalis (n 1) в группе контроля.
b В результатах БАЛ Staphylococcus aureus (n 1), Enterococcus faecium (n 2),
Streptococcus pneumoniae (n 3), influenza A (n 3), Aspergillus fumigatus (n 1) в
группе CytoSorb. В группе контроля: influenza A (n 2), Candida albicans (n 1),
Pseudomonas aeruginosa (n 1), и Serratia marcescens (n 1).
Критерии исключения
Из исследования исключались пациенты младше 18 лет, беременные, пациенты с кардиогенным шоком и противопоказаниями к экстракорпоральной терапии (коагулопатия, тромбоцитопения). У всех пациентов зарегистрирован ОРДС, проводилась терапия согласно рекомендациям по терапии сепсиса. Стандартная терапия включала в себя водную нагрузку, дифференцированную катехоламиновую поддержку, включающую назначение норэпинефрина для достижения среднего артериального давления (САД) 60 мм рт. ст., антибактериальную терапию с учетом резистентности и протективную вентиляцию. Первичной конечной точкой исследования была 30-суточная летальность. Вторичные конечные точки: продолжительность пребывания в ОРИТ, изменения концентраций маркеров инфекционного поражения (СРБ, лейкоциты и ПКТ сыворотки), концентрация лактата, потребность в вазопрессорах до начала ЭКМО/CytoSorb, через 12, 24, 48 и 72 часа после начала процедуры ЭКМО/CytoSorb. Кроме того, баллы по шкале SAPS II регистрировались при поступлении в ОРИТ, затем на 1-е, 2-е и 3-и сутки после поступления для оценки вероятности летального исхода в обеих группах.
Показанием к началу ЭКМО являлось клиническое ухудшение на фоне острой респираторной недостаточности. Всем пациентам после поступления в ОРИТ в течение 12 часов после постановки диагноза септический шок начинали периферическую высокопоточную вено-венозную ЭКМО в комбинации с иммуномодуляцией CytoSorb. Оценка сердечной функции до начала ЭКМО проводилась с помощью трансторакальной эхокардиографии. Во время процедуры выполнялась системная продленная внутривенная антикоагуляция аргатробаном (АЧТВ 50-60 секунд). Показанием к назначению для CytoSorb служила сепсис- ассоциированная гемодинамическая нестабильность с высокой потребностью в катехоламинах (0.3 мкг/кг/мин). Система CytoSorb устанавливалась в контур ЭКМО. Все пациенты получили минимум два сеанса терапии CytoSorb. Адсорберы меняли каждые 24 часа без промежутков между сессиями терапии CytoSorb. Терапию CytoSorb продолжали до тех пор, пока потребность в инфузии катехоламинов сохранялась, или до выхода из шока.
Статистический анализ
Данные анализировались с помощью статистической программы GraphPad Prism 7 (GraphPad Software, США). Результаты с p 0.05 признавались статистически значимыми.
Результаты
Тринадцать пациентов с пневмогенным сепсисом и ОРДС (группа CytoSorb) соответствовали критериям включения и вошли в исследование. В исторической когорте было идентифицировано 7 пациентов с пневмогенным сепсисом и ОРДС, которым проводили ЭКМО. Их данные подверглись ретроспективному анализу (группа контроля). Средний возраст пациентов 61±3 года (диапазон 32-76) в группе CytoSorb и 61±2 года (39-71) в контрольной группе. У пяти пациентов в группе CytoSorb и четырех пациентов в контрольной группе развилась анурическая почечная недостаточность с потребностью в продленном вено-венозном гемодиализе. Последующий анализ бронхиального секрета, полученного в ходе бронхоскопии, указывал на развитие гриппозной пневмонии у трех пациентов, грибковой пневмонии у одного пациента и бактериальной пневмонии у девяти пациентов
(►Таблица 1).
30-суточная летальность
Уровень 30-суточной летальности составил 0% в группе CytoSorb по сравнению с 57% (4 из 7 пациентов) в группе контроля. Причиной летальных исходов в контрольной группе стала эскалация сепсиса и развитие ПОН. Стоит отметить, что уровень выживаемости в группе CytoSorb и далее (по прошествии 6±2.5 месяцев; диапазон отслеживания: от 3 до 10 месяцев) сохранился на отметке 100%.
Шкала SAPS II
При поступлении в ОРИТ средний балл по шкале SAPS II составил 58±2 (диапазон: 49-66) в группе CytoSorb и 50±2 (42-55) в группе контроля (доверительный интервал 95%: от 15.75 до 1.85, p 0.02). После начала терапии CytoSorb балл по шкале SAPS II значительно снижался в 1-е (43±4, p 0.004), затем во 2-е сутки (41±4, p 0.0006) и на 3-и сутки (30±4, p 0.0001), что указывало на снижение риска летальности в группе CytoSorb. В группе контроля, напротив, мы не наблюдали заметных изменений по шкале SAPS II на 1-е, 2-е и 3-и сутки в ОРИТ.
С-реактивный белок
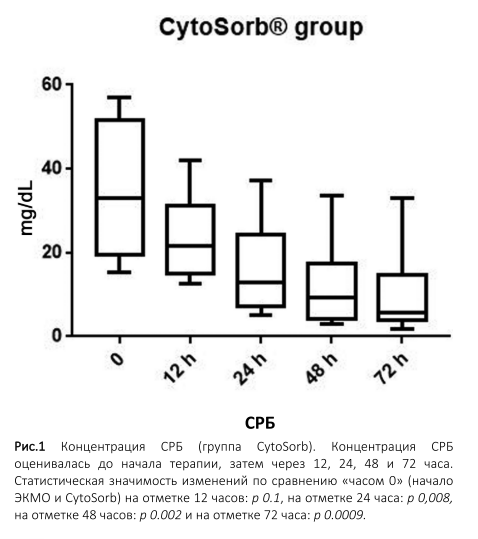
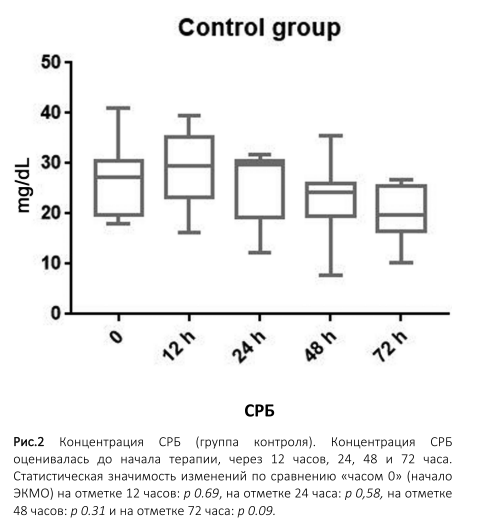
Изначально высокие концентрации C-реактивного белка (СРБ0 35±5, диапазон: 15-57) снизились за время процедуры ЭКМО/CytoSorb через 12 часов (СРБ12 24±3, p 0.1), 24 часа (СРБ24 16±3, p 0,008), 48 часов (СРБ48 12±3, p 0.002)и 72 часа (СРБ72 10±3, p 0.0009), соответственно (►Рис. 1). В группе контроля, напротив, снижения концентрации СРБ не наблюдалось (СРБ0 27.2±2.9; СРБ12 29±3.3, p 0.69; СРБ24 25.01±2.8, p 0,58; СРБ48 22.6±3.1, p 0.31; СРБ72 20.02±2.4, p 0.09).
Прокальцитонин
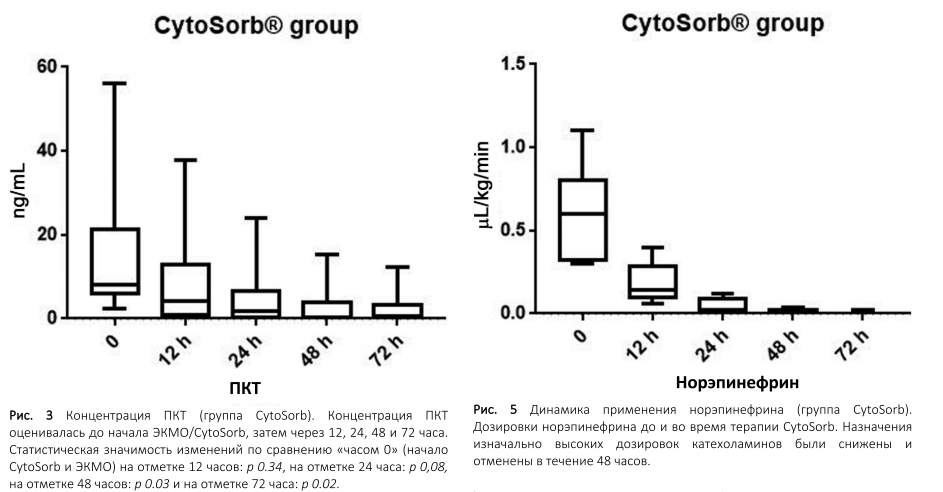
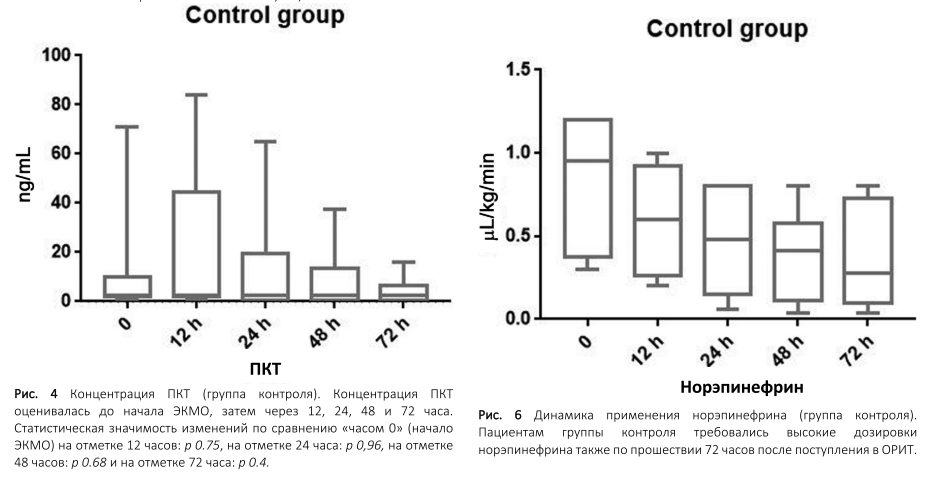
Снижение концентрации прокальцитонина отмечалось через 12 часов после начала терапии ЭКМО/CytoSorb (ПКТ12 9.05±3.9 нг/мл, p 0,34), 24 часа (ПКТ24 4.71±2.3 нг/мл, p 0,08), 48 часов (ПКТ48 2.71±1.5 нг/мл, p 0,03), и 72 часа (ПКТ72 2.3±1.2 нг/мл, p 0,02), соответственно, по сравнению с изначально высокими значениями, зарегистрированными до начала терапии (ПКТ0 15.6±5.4 нг/мл, диапазон 2.5 – 56.04 нг/мл) (►Рис. 3). В контрольной группе после начала ЭКМО не наблюдалось заметной разницы в уровнях концентрации ПКТ (ПКТ0 13.14±9.7 нг/мл, диапазон 1.18 – 70.81 нг/мл; ПКТ12 18.95±16.32 нг/мл, p 0,75; ПКТ24 12.5±10.5 нг/мл, p 0,96; ПКТ48 8.14±5.9 нг/мл, p 0,68; ПКТ72 4.1±2.4 нг/мл, p 0,4) (►Рис. 4).
Лейкоциты
В обеих группах не продемонстрировано заметное снижение количества лейкоцитов на отметках 12, 24, 48 и 72 часа.
Изменение потребности в норэпинефрине за время терапии
Средние дозировки норэпинефрина на момент начала терапии составляли 0.603±0.08 мкг/кг/мин (диапазон: 0.3-1.1 мкг/кг/мин) в группе CytoSorb и 0.83±0.16 мкг/кг/мин (диапазон 0.3-1.2 мкг/кг/мин) в контрольной группе (95% доверительный интервал: 0.2016-0.5556, p 0.3309). Важно отметить, что в группе CytoSorb потребность в норэпинефрине значительно сократилась через 12, 24, 48 часов терапии по сравнению с изначальным назначением (12 часов: 0.19±0.04 мкг/кг/мин, p 0.0002; 24 часа:
0.045±0.01 мкг/кг/мин, p 0.0001; 48 часов: 0.009±0.005 мкг/кг/мин, p 0.0001). По прошествии 72 часов поддержка норадреналином пациентам более не требовалась (►Рис. 5). В группе контроля высокая потребность в норадреналине сохранялась через 12 часов (0.6±0.13 мкг/кг/мин, p 0.28), 24 часа (0.47±0.14 мкг/кг/мин, p 0/12), 48 часов (0.38±0.11 мкг/кг/мин, p 0.05), 72 часа (0.37±0.13 мкг/кг/мин, p 0.05), соответственно, после поступления в ОРИТ (►Рис. 5).
Лактат
В группе CytoSorb мы наблюдали впечатляющее снижение концентрации лактата через 12 часов (2.1±0.57 ммоль/л, p 0.02) и 72 часа (1.1 ± 0.3 ммоль/л, p 0.009) по сравнению с изначальными значениями (4.1 ± 0.97 ммоль/л, диапазон: 2.1 – 12.4 ммоль/л). В группе контроля, напротив, снижения концентрации лактата не отмечалось (начальный уровень 2.7 ± 0.34 ммоль/л, диапазон: 2- 4,4 ммоль/л, на отметке 12 часов: 1.57 ± 0.5 ммоль/л, p 0/08; на отметке 48 часов: 1.7 ± 2.9 ммоль/л, p 0.05; через 72 часа: 2 ± 0.37
ммоль/л, p 0.18).
Продолжительность экстракорпоральной поддержки
Средняя продолжительность ЭКМО в группе CytoSorb составила 8 ± 2 суток (диапазон 2-23 суток), в группе контроля продолжительность ЭКМО составила 19 ± 3 суток (диапазон: 13- 30 суток). У семи пациентов применено три сеанса иммуномодулирующей терапии, потребность в которой нивелировалась через 3 суток. Трое пациентов получали терапию CytoSorb непрерывно в течение двух суток. Скорость кровотока поддерживалась на уровне от 200 до 400 мл/мин и мониторировалась с помощью датчика потока. Мы не наблюдали нежелательных событий, связанных с терапией или адсорбером. Средняя продолжительность пребывания в ОРИТ составила 26±6 суток (диапазон 7 63 дня) в группе CytoSorb и 26±5 суток (диапазон: 8-43 дня) в группе контроля. Все пациенты были переведены из ОРИТ в другие отделения для восстановительного лечения.
Обсуждение
Безотлагательная терапия сепсиса важна для предупреждения нарастания тяжести состояния и предотвращения летальных исходов. Кроме прочего, цитокины, ПКТ и СРБ являются маркерами воспалительной реакции, обладающими высокой диагностической и прогностической ценностью.11 СРБ – широко описанный маркер, служащий для детекции и мониторинга септических состояний.12 В последнее время ПКТ стал более популярен, чем СРБ, в части диагностики, мониторинга и
прогноза клинических исходов сепсиса и септического шока.11,13 Кроме того, описана высокая корреляция концентраций провоспалительного цитокина интерлейкин-6, продуцируемого во время острой фазы воспаления, с тяжестью септических состояний и прогнозом развития септических осложнений.11,14 Концентрация лактата сыворотки служит индикатором латентныхшоковых состояний и помогает отслеживать ответную реакцию на проводимую терапию.15
В нашем исследовании пациентам с ОРДС на фоне тяжелого течения пневмонии и пневмогенного сепсиса проводилась высокопоточная вено-венозная ЭКМО в комбинации с иммуномодулирующей терапией. Показатели исторической группы контроля анализировались ретроспективно. Примечательно раннее значительное снижение СРБ и ПКТ когорте CytoSorb. Рассчитанный по шкале SAPS II риск летальности после гемосорбции был ниже, чем риск летальности в контрольной группе. Терапия CytoSorb привела к стреми тельной стабилизации гемодинамики и снижению уровня лактата. Во время терапии CytoSorb у всех пациентов отмечено значительное снижение потребности катехоламинах, все пациенты этой группы выжили, в то время как в группе контроля зарегистрировано четыре летальных исхода из семи. Септический шок и тяжелый сепсис, сопровождающийся повышением концентраций цитокинов, являются одними из основных показаний к применению системы CytoSorb, доступной в клинической практике и считающейся в настоящее время безопасной и хорошо переносимой пациентами. Применение CytoSorb кардиохирургических пациентов.9,16 описано также при тяжелом ССВО у
Провоспалительные цитокины, включая фактор некроза опухоли альфа и интрелeйкин-6 эффективно удаляются из крови во время терапии CytoSorb. Эта сорбционная методика оказывает положительное влияние на гемодинамическую стабильность путем снижения потребности в вазопрессорной поддержке и сокращает концентрации медиаторов воспаления в плазме крови пациентов с сепсисом.6,17 Несмотря на то, что мы не измеряли изменения концентраций цитокинов во время терапии CytoSorb, мы смогли продемонстрировать снижение уровней СРБ, ПКТ и лактата, а также резкое сокращение потребности в вазопрессорной поддержке в течение первых 12 часов терапии по сравнению с группой контроля. Наши заключения, таким образом, перекликаются с другими исследованиями, которые свидетельствуют о том, что применение CytoSorb признается эффективным для стабилизации гемодинамики, снижения потребности в вазопрессорной поддержке, повышения клиренса лактата в контексте сепсиса и септического шока и впоследствии ведет к благоприятному клиническому исходу.
Несколько клинических исследований продемонстрировали благоприятный эффект терапии CytoSorb в части снижения интенсивности воспалительного ответа. В недавнем исследовании Friesecke et al терапия пациентов с рефрактерным септическим шоком с помощью CytoSorb привела к снижению потребности в норэпинефрине через 6 и 12 часов, а также к повышению клиренса лактата и выходу из септического шока у 65% пациентов. В этом исследовании CytoSorb использовался в контуре почечной заместительной терапии. 18 В серии клинических случаев, описанной Kogelmann et al, наблюдаемая летальность была ниже расcчитанной по шкале APACHE II.19 Примечательно, что эффективность терапии была выше у пациентов, которым CytoSorb применяли в течение 24 часов с момента диагностики сепсиса по сравнению с пациентами, терапию CytoSorb которым начинали позднее, чем 24 часа с момента постановки диагноза. В нашем исследовании мы начинали комбинированную терапию ЭКМО/CytoSorb в течение 6 часов с момента поступления пациента в ОРИТ и в течение 12 часов с момента диагностики сепсиса для достижения наилучшего эффекта в соответствии с ограниченным количеством данных, имеющихся на момент исследования. До настоящего времени применение CytoSorb описано, в основном, у пациентов с кардиогенным сепсисом. В ретроспективной серии клинических случаев Träger et al описывал применение CytoSorb у 16 пациентов после кардиохирургического вмешательства с долгим временем нахождения на искусственном кровообращении и развитием обширного постоперационного ССВО с последующим ОПП. Терапия CytoSorb у этих пациентов ассоциировалась со стабилизацией гемодинамики, метаболизма и функционирования органов.5 Bruenger et al описывал успешное применение CytoSorb в комбинации в устройством поддержки левого желудочка и
правожелудочковым ЭКМО у пациента с ОРДС и септической кардиогенной недостаточностью. В работе продемонстрировано снижение интерлейкина-6 и ПКТ в плазме крови, а также сокращение потребности в вазопрессорах. В этом отдельно взятом случае CytoSorb работал в контуре продленной вено-венозной гемофильтрации. Одно из крупнейших ретроспективных клинических исследований включало 39 пациентов кардиохирургического профиля с подтвержденным острым инфекционным эндокардитом, которым проводилось вмешательство по замене клапанов с использованием искусственного кровообращения и проводилась интраоперационная гемосорбция CytoSorb. Это исследование отражает преимущества подобного подхода в части снижения концентрации цитокинов (интерлейкин- 6 и интерлейкин-8) и стабилизации гемодинамики по сравнению с исторической группой из 28 пациентов, которым не применялась интраоперационная гемосорбция.20
Как известно, ЭКМО сама по себе ведет к развитию воспалительного ответа, активируя систему комплемента и вызывая рост концентраций провоспалительных цитокинов.4 Последние активируют эндотелий сосудов, а ненатуральные внутренние поверхности магистралей ЭКМО и мембран могут усиливать воспалительную реакцию и, в конечном итоге, катализировать органные повреждения. Сочетание септических процессов и активации иммунного ответа на фоне ЭКМО могут
привести к развитию системного гипервоспаления с развитием гемодинамической нестабильности.21 В нашем исследовании стабилизация гемодинамики проявлялась как снижение потребности в норадреналине в течение 48 часов во время применения комбинации ЭКМО и CytoSorb. Этого не происходило в контрольной группе, и это наблюдение указывает на непрямые эффекты адсорбции цитокинов в части достижения гемодинамической стабилизации на ранних этапах развития сепсиса. Ограничением этого исследования является малое число пациентов в обеих группах и отсутствие проспективной рандомизации пациентов в группе контроля. В настоящей работе мы описали наш опыт применения сорбции цитокинов. Целью настоящего исследования являлась оценка роли этой новой технологии в терапии пневмогенного сепсиса и снижении летальности. Несмотря на то, что благоприятные эффекты применения комбинации ЭКМО и CytoSorb отразились в снижении летальности в группе CytoSorb, небольшое число пациентов ограничивает возможности сравнения групп. Более того, мы не проводили измерений концентраций цитокинов, снижение которых является основной целью гемосорбции. Насколько нам известно, это первое исследование пациентов с тяжелым пневмогенным сепсисом и ОРДС, которым успешно применяли комбинацию высокопоточного вено- венозного ЭКМО и сорбции цитокинов. Интригующие данные, полученные в ходе настоящего исследования, нуждаются в дальнейшем изучении в многоцентровых проспективных исследованиях, включающих пациентов с ОРДС и пневмогенным сепсисом.
Конфликт интересов.
Отсутствует.
Ссылки
1 CrowtherMA, Marshall JC. Continuing challenges of sepsis research.JAMA 2001;286(15):1894–1896
2 Singer M, Deutschman CS, Seymour CW, et al. The third international consensus definitions for sepsis and septic shock (Sepsis-3). JAMA 2016;315(08):801–810
3 Pranikoff T, Hirschl RB, Steimle CN, Anderson HL III, Bartlett RH. Efficacy of extracorporeal life support in the setting of adult cardiorespiratory failure. ASAIO J 1994;40(03):M339–M343
4 Millar JE, Fanning JP, McDonald CI, McAuley DF, Fraser JF. The inflammatory response to extracorporeal membrane oxygenation (ECMO): a review of the pathophysiology. CritCare 2016;20(01):387
5 Träger K, Fritzler D, Fischer G, et al. Treatment of post- cardiopulmonary bypass SIRS by hemoadsorption: a case series. Int J Artif Organs 2016;39(03):141–146
6 Song M, Winchester J, Albright RL, Capponi VJ, Choquette MD, Kellum JA. Cytokine removal with a novel adsorbent polymer. Blood Purif 2004;22(05):428–434
7 Mitzner SR, Gloger M, Henschel J, Koball S. Improvement of hemodynamic and inflammatory parameters by combined hemoadsorption and hemodiafiltration in septic shock: a case report. Blood Purif 2013;35(04):314–315
8 BruengerF, Kizner L,Weile J,MorshuisM, Gummert JF. First successful combination of ECMO with cytokine removal therapy in cardiogenic septic shock: a case report. Int J Artif Organs 2015;38(02):113–116
9 Friesecke S, Träger K, Schittek GA, et al. International registry on the use of the CytoSorb® adsorber in ICU patients: study protocol and preliminary results. Med Klin Intensivmed Notfmed 2019; 114(08):699–707
10 Houschyar KS, Pyles MN, Rein S, et al. Continuous hemoadsorption with a cytokine adsorber during sepsis - a review of the literature. Int J Artif Organs 2017;40(05):205–211
11 Akil A, Reichelt J, Ziegeler S, Semik M, Fischer S. Combined use of cytokine adsorption therapy and extracorporeal membrane oxygenation (ECMO) in patients with severe pneumogenic sepsis and acute respiratory distress syndrome (ARDS). 27th European Conference on General Thoracic Surgery; Dublin, Ireland 2019:173–174
12 Tan M, Lu Y, Jiang H, Zhang L. The diagnostic accuracy of procalcitonin and C-reactive protein for sepsis: a systematic review and meta-analysis. J Cell Biochem 2019;120(04):5852 5859
13 Becker KL, Snider R, Nylen ES. Procalcitonin assay in systemic inflammation, infection, and sepsis: clinical utility and limitations. Crit Care Med 2008;36(03):941–952
14 Oberholzer A, Souza SM, Tschoeke SK, et al. Plasma cytokine measurements augment prognostic scores as indicators of outcome in patients with severe sepsis. Shock 2005;23(06):488–493
15 Ding XF, Yang ZY,Xu ZT, et al. Early goal-directed and lactate-guided therapy in adult patients with severe sepsis and septic shock: a meta-analysis of randomized controlled trials. J TranslMed2018;16 (01):331
16 Baumann A, Buchwald D, Annecke T, Hellmich M, Zahn PK, Hohn A. RECCAS - REmoval of Cytokines during CArdiac Surgery: study protocol for a randomised controlled trial. Trials 2016;17(01):137
17 Morris C, Gray L, Giovannelli M. Early report: the use of Cytosorb™ haemabsorption column as an adjunct in managing severe sepsis: initial experiences, review and recommendations. J Intensive Care Soc 2015;16(03):257–264
18 Friesecke S, Stecher SS, Gross S, Felix SB, Nierhaus A. Extracorporeal cytokine elimination as rescue therapy in refractory septic shock: a prospective single-center study. JArtifOrgans 2017;20(03):252–259
19 Kogelmann K, Jarczak D, Scheller M, Drüner M. Hemoadsorption by CytoSorb in septic patients: a case series. Crit Care 2017;21(01):74
20 Träger K, Skrabal C, Fischer G, et al. Hemoadsorption treatment of patients with acute infective endocarditis during surgery with cardiopulmonary bypass - a case series. Int J Artif Organs 2017;40 (05):240–249
21 McILwain RB, Timpa JG, Kurundkar AR, et al. Plasma concentrations of inflammatory cytokines rise rapidly during ECMO-related SIRS due to the release of preformed stores in the intestine. Lab Invest 2010;90(01):128–139
Ключевые слова: экстракорпоральная мембранная оксигенация, ЭКМО, воспаление системное; на клеточном уровне, медиаторы, шок; генерализация, сердечно-сосудистый, циркуляторный

