Первая успешная комбинация экстракорпоральной мембранной оксигенации (ЭКМО) с терапией удаления цитокинов при кардиогенном септическом шоке: отчет о клиническом случае
First successful combination of ECMO with cytokine removal therapy in cardiogenic septic shock: A case report
Frank Bruenger 1, Lukasz Kizner 1, Jan Weile 2, Michael Morshuis 1, Jan F. Gummert 1
1 Клиника торакальной и сердечно-сосудистой хирургии, Центр сердца и диабета Северной Рейн-Вестфалии, Бад-Эйнхаузен – Германия
2 Институт лабораторной и трансфузионной медицины, центр сердца и диабета Северной Рейн-Вестфалии, Бад-Эйнхаузен – Германия
Опубликовано в журнале International Journal of Artificial Organs 2015; 00(00):000-000. DOI: 10.5301/ijao.5000382
КРАТКИЙ ОБЗОР
Цель: Новая система для гемоадсорбции, предназначенная для дополнительной терапии пациентов с повышенными уровнями цитокинов в условиях синдрома системного воспалительного ответа (ССВО) и сепсиса показала многообещающие результаты. Мы докладываем о благоприятных результатах применения системы у пациента с кардиогенным шоком, получающего комбинированную экстракорпоральную поддержку с помощью экстракорпоральной мембранной оксигенации (ЭКМО), устройства для механической поддержки левого желудочка и постоянной вено-венозной гемофильтрации, несмотря на септическое состояние пациента.
Методы: у 39-летнего пациента выявлен фульминантный острый респираторный дистресс-синдром (ОРДС) и кардиогенный септический шок. Для циркуляторной поддержки применялось вено-артериальное ЭКМО. Во время течения болезни в дополнение к хронической почечной недостаточности у пациента развилась острая почечная недостаточность, в связи с чем пришлось начать постоянную вено-венозную гемофильтрацию. Поскольку произошла остановка сердечной деятельности (оба желудочка), было имплантировано устройство для механической поддержки левого желудочка в комбинации с вено-венозным (правым) ЭКМО, несмотря на сепсис. После операции уровень IL-6 и дозировка вазопрессоров резко повысились. В связи с этим в контур аппарата для вено-венозной гемофильтрации поместили систему CytoSorb, и в последующие 4 дня было проведено 3 сессии.
Результаты: Во время терапии CytoSorb маркеры воспаления IL-6, прокальцитонин, С-реактивный белок снизились конкоминантно с потребностью в вазопрессорах. Не было зарегистрировано неблагоприятных эффектов, связанных с системой CytoSorb, во время или после сессий терапии.
Выводы: Это первый отчет о клиническом случае, когда пациента с тяжелым сепсисом назначили комбинированную терапию с применением устройства для механической поддержки левого желудочка, вено-венозного (правого) ЭКМО, постоянной вено-венозной гемофильтрации и системы CytoSorb. Вышеуказанная комбинация имела практическое значение, была технически осуществима и высоко эффективна. Комбинация представляет собой разумный подход для улучшения выживаемости пациентов с полиорганной недостаточностью, требующей поддержки нескольких органов.
Ключевые слова: Септический шок, гемосорбция, CytoSorb, устройство для механической поддержки левого желудочка, ЭКМО, постоянная вено-венозная гемофильтрация.
*****************************************************************
Предпосылки
Системное воспаление и сепсис могут сопровождаться ОРДС, в связи с чем в отделениях интенсивной терапии (ОИТ) в качестве органо-поддерживающей терапии часто используют ЭКМО. (1) Механизмы, ведущие к капиллярной утечке и последующее развитие отека легких до настоящего момента до конца не понятны, тем не менее, цитокины и их непропорциональное выделение во время системного воспаления, кажется, играют решающую роль в этом процессе.(2,3) С этой точки зрения кажется разумным контролировать воспалительный ответ и оказывать пациенту поддержку до тех пор, пока не ослабнет воспаление, и не восстановится оксигенация легких. Новая система для гемоадсорбции, предназначенная для дополнительной терапии пациентов с повышенными уровнями цитокинов в условиях синдрома системного воспалительного ответа (ССВО) и сепсиса, показала многообещающие результаты при лечении септических пациентов. Она также успешно применялась в качестве средства терапии в других случаях повышения уровней концентрации цитокинов (например, в общей кардиохирургии с применением аппаратов искусственного кровообращения)(8). Таким образом, система представляет собой обнадеживающий инструмент для решения подобной проблемы. В настоящем отчете о клиническом случае мы рассматриваем пациента с дисфункцией нескольких органов и потребностью в многочисленных органо-поддерживающих мероприятиях из-за фульминантного ОРДС и кардиогенного септического шока. Пациенту была проведена дополнительная терапия с помощью CytoSorb. Одобрение этического комитета для данного исследования не потребовалось; было получено информированное согласие от родственников пациента.
Презентация клинического случая
Пациент: мужчина, 39 лет, в анамнезе дилатационная кардиомиопатия (фракция изгнания левого желудочка – 20%) одиопатической этиологии, с 2006 до 2012 года регулярно проходил обследование в медицинском учреждении. Дальнейшая история болезни включала вторичную легочную гипертензию, недостаточность митрального клапана от 2 до 3 степени, хроническую почечную недостаточность в стадии компенсированной ретенции, гипотиреоз и злоупотребление никотином и анаболиками. В 2006 году пациенту был имплантирован двухкамерный кардиовертер-дефибриллятор, в январе 2007 года было принято решение о плановой трансплантации.
В январе 2013 года пациент провел в стационаре 3 дня во время рутинной диспансеризации. Спустя неделю пациент обратился в другую больницу с диспноэ. После неинвазивной вентиляции легких состояние пациента резко ухудшилось, он был интубирован и переведен на искусственную вентиляцию легких (ИВЛ). Проведенное ренгеновское исследование подтвердило наличие двусторонних массивных инфильтратов. В течение нескольких часов у пациента развился фульминантный ОРДС и кардиогенный септический шок (лейкоциты 18700/μл, С-реактивный белок 18 мг/дл, прокальцитонин 52 нг/мл); для стабилизации гемодинамики была назначена высокая доза катехоламинов (ноэпинефрин 6-8 мг/час, эпинефрин 5-8 мг/час, среднее артериальное давление 55-60 мм рт. ст.).
После телефонного звонка из больницы, в которую госпитализировали пациента, наша команда на базе больницы, в которую он был госпитализирован, имплантировала ему вено-артериальное ЭКМО через бедренную артерию, после чего пациента перевезли в наш Центр. В дальнейшем в виду подозрений на грипп базовая терапия осуществлялась с помощью препарата тамифлу (Tamiflu) в течение 4 дней. В отделение ОИТ ИВЛ осуществялась в режиме контроля по давлению, сразу же начали терапию антибиотиками: линезолид (Linezolid), меропенем (Meropenem), моксифлоксацин (Moxifloxacin), вориконазол (Voriconazol) и ацикловир (Acyclovir). Потребность в катехоламинах в последующие дни значительно снизилась (норэпинефрин 0.5 мг/ч, эпинефрин 0.4 мг/час, вазопрессин 0.04 ед/час, среднее вартериальное давление 65-70 мм рт. ст.). Проведенный через двое суток бронхоальвеолярный лаваж подтвердил колонизацию viridans streptococci, однако, полимеразцная цепная реакция (ПЦР) не выявила вируса гриппа.
Во время лечения у пациента развилась острая почечная недостаточность в дополнение к его хронической почечной недостаточности. Повысились уровни креатинина и мочевины в плазме (Таблица 1), а также снизилась экскреция мочи (данные не представлены).
Таблица 1.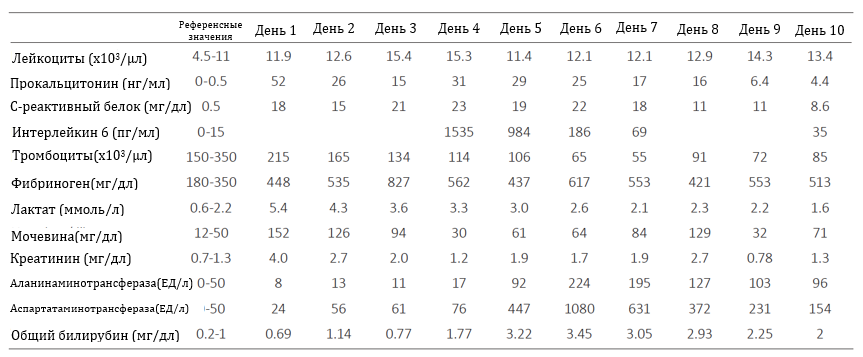
В дополнение несмотря на значительный положительный жидкостный баланс (около 10 л), смещение баланса в отрицательную сторону с помощью диуретиков оказалось невозможным (этакриновая кислота, фуросемид внутривенно). Была начата непрерывная веновенозная гемофильтрация, что привело к нормализации концентрации креатинина и мочевины (Таблица 1) в течение последующих дней. Однако в связи с глобальной (бивентрикулярной) акинезией сердца и высоким риском внутрисердечного тромбоза мы решили имплантировать левожелудочковый обход LVAD; Heartware, Framigham, MA, USA) в комбинации с правосторонним ЭКМО (rECMO, Centimag; Thoratec, Pleasanton, CA USA) заменив ими веноартериальное ЭКМО для обеспечения раздельной поддержки левого и правого желудочков и стабилизации гемодинамики. Для обеспечения этого комбинированного вмешательства была произведена стернотомия. Контур ЭКМО был подключен между полой веной (бедренная венозная канюля, проведенная до уровня правого предсердия) и легочной артерией (посредством анастомоза «конец-в-бок» с 8 мм протезом Hemashield, к которому в свою очередь была присоединена стандартная канюля). Левожелудочковый обход был подключен между верхушкой левого желудочка и восходящей аортой.
Что важно, хирургическое вмешательство было проведено несмотря на сепсис. Послеоперационное состояние пациента ожидаемо ухудшилось в последующие несколько часов, создавая потребность в высоких дозировках вазопрессоров (норэпинефрин 2 мг/час, эпинефрин 1 мг/час, вазопрессин 0.32 ЕД/час). Ухудшение состояния и развитие лейкоцитоза (15300/μл), а также чрезмерное повышение уровня концентрации интерлейкина 6 в плазме крови (1535 пг/мл) и высокий уровень лактата (3.3 ммоль/л) указывали на развитие тяжелого сепсиса.
В качестве последнего средства в контур аппарата для постоянной вено-венозной гемофильтрации (AK200; Gumbro, Лунд, Швеция), был подключен CytoSorb (Штаб-квартира CytoSorbents Europe, Берлин, Германия). Адсорбер CytoSorb подключали сериями, размещая в контуре перед гемофильтром, от CytoSorb к пациенту шел катетер Шелдона, установленный во внутреннюю яремную вену. Сессии терапии CytoSorb проводились в 1-ый, а также во 2-ой и 4-ый дни после операции. Длительность сессий составляла от 18 до 21 часов. Скорость кровотока варьировалась от 155 мл/мин до 240 мл/мин, антикоагуляция выполнялась с помощью гепарина для поддержания частичного активированного частичного тромбопластинового времени (АЧТВ) в диапазоне от 60 до 80, мониторинг АЧТВ проводился каждые 4 часа. Кроме этого, каждые 8 часов анализировалось содержание ATIII, фибриногена и количество тромбоцитов, при необходимости выполняли их замещение. Важно отметить, что прямая установка CytoSorb в контур ЭКМО опасна риском аспирации и течи контура, и, таким образом, строго противопоказана.
Рис.1 Режимы терапии и тренд уровней IL-6, прокальцитонина и С-реактивного белка до, во время и после терапии CytoSorb.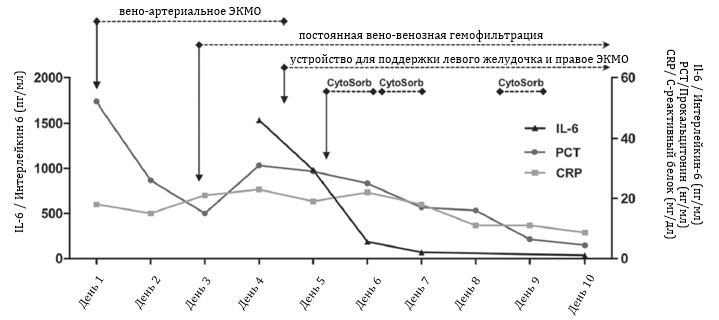
Рис.2 Режимы терапии и и уровни потребности в вазопрессорах до, во время и после терапии CytoSorb. 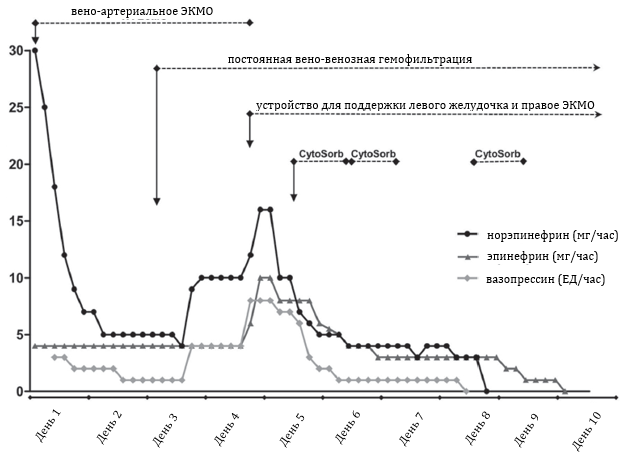
За весь период терапии (4 дня) пациент получал линезолид, меропенем, моксифлоксацин, кориконазол и ацикловир в виде болюсных введений. Адаптации дозировки за время время лечения не проводилось. С началом терапии CytoSorb в комбинации с ЭКМО маркеры воспаления (интерлейкин 6, прокальцитонин и С-реактивный белок) существенно снизились во время лечения и продолжили снижаться в течение последующих дней (Рис.1). Кроме того, нам удалось значительно снизить дозировку вазопрессоров и совсем прекратить их применение во время (норэпинефрин и вазопрессин) и через некоторое время после последней сессии (эпинефрин) терапии CytoSorb (Рис. 2). Важно отметить, что не было зарегистрировано никакого отрицательного влияние на количество тромбоцитов, а дозировку антибиоткиов не пришлось кореектировать на протяжении всей продолжительности терапии CytoSorb и после нее. Вено-венозное (правое) ЭКМО отключили через 19 дней, а отлучение от ИВЛ провели спустя 27 дней после окончания терапии. Для регенерации почек пациент находился на продолжительной вено-венозной гемофильтрации еще 21 день, и был выписан из ОИТ на 38 день, а из стационара – на 76 день после последней сессии терапии CytoSorb в комбинации с устройством для механической поддержки левого желудочка. Пациент все еще числится в очереди на трансплантацию.
Выводы
Это первый отчет о клиническом случае, где для терапии применялась комбинация устройства для механической поддержки левого желудочка, вено-венозного (правого) ЭКМО, постоянной вено-венозной гемофильтрации и CytoSorb. Вышеуказанная комбинация имела практическое значение, была технически осуществима и очень благотворна для пациента. Не было зарегистрировано неблагоприятных эффектов, связанных с системой CytoSorb, во время или после сессий терапии. Ввиду того, что терапия пациента была многоуровневой, включала в себя клиническую и фармакологическую поддержку, кажется амбициозным заявлять, что система CytoSorb явилась залогом успешного лечения. Однако, так как состояние пациента сильно ухудшилось после проведения обширного хирургического вмешательства, у пациента был септический шок, а дозировки вазопрессоров - оченьвысокими, мы решили применить CytoSorb в качестве последнего средства. После начала терапии CytoSorb воспалительный статус пациента улучшился, вазопрессорную поддержку возможно стало сократить, а вскоре и отменить. Это соответствует другим отчетам о клинических случаях и клиническим исследованиям, в которых сообщается о подобных эффектах, оказываемых на воспаление и клинический исход (4-8).
Стоит отменить, что ранее в литературе были описаны некоторые другие позитивные результаты гемоадсорбции. Пенг (Peng) и его коллеги на живтоных моделях с абдоминальным сепсисом (каловый перитонит) продемонстрировали возможность системы CytoSorb не только эффективно снижать уровни цитокинов, но также оказывать положительный эффект на гемодинамику (улучшение среднего артериального давления) и кратковременную выживаемость (9). Та же группа определила, что гемоадсорбция с помощью CytoSorb может снизить синтез de novo медиаторов воспаления и даже остановить и предотвратить цитокино- и медитор- индуцированнное повреждение тканей (10).
Более того, благодаря исследованиям на животных есть доказательства того, что гемоадсорбция может оказывать прямое влияние на клеточный иммунный ответ путем модуляции хемокиновых градиентов и перенаправления траффика лейкоцитов к месту воспаления (11,12).
Таким образом, систему CytoSorb можно применять в комбинации с ЭКМО – это приносит значительную пользу пациенту, и таким образом, является разумным подходом для улучшения выживаемости пациентов с дисфункцией нескольких органов и потребностью в нескольких органо-поддерживающих видах лечения.
Похожие публикации по теме:
- Продленная гемоадсорбция в контуре ЭКМО для купирования посткардиотомного кардиогенного и септического шока. Клинический случай
- Успешное применение экстракорпорального жизнеобеспечения (ваЭКМО), внутривенной инфузии липидов и CytoSorb при интоксикации венлафаксином и кардиомиопатии такоцубо
- Терапия сепсиса и свиного гриппа с помощью ЭКМО и CytoSorb Комбинация ЭКМО и адсорбции цитокинов при терапии тяжелого сепсиса, осложненного кардиогенным шоком и ОРДС
- Применение гемоадсорбционной колонки в контуре педиатрической системы ЭКМО

